曾园山教授团队关于构建独特微环境的类脊髓白质促进轴突直行再生及成髓鞘修复脊髓损伤的研究在《Bioactive Materials》发表
脊髓损伤给家庭和社会带来沉重的负担,脊髓损伤修复是世界性的医学难题,也是我国科技计划重点攻克的科学问题。脊髓损伤后在损伤处形成不利于神经再生的微环境,神经元轴突(神经纤维)的内在再生能力受限;持续存在的炎症反应最终导致损伤处形成胶质和纤维瘢痕,发展为难于逆转的感觉和运动功能障碍。重塑脊髓神经再生微环境,促进轴突及其髓鞘再生,最终重建脊髓神经环路是攻克脊髓损伤修复难题的关键。
近十几年来国内外研究发现,单纯细胞移植很难实现干细胞在脊髓复杂损伤微环境中定向分化为功能细胞。然而,组织工程策略优势在于可以根据脊髓修复的具体需求,设计支架材料、种子细胞和生物活性因子的最优组合,以应对如何重塑神经再生微环境和修复脊髓神经环路的关键科学问题。
我重点实验室曾园山教授团队长期致力于应用干细胞和组织工程策略修复受损伤脊髓的神经环路,对作为组织工程要素之一的生物支架材料实施持续研发。在脊髓损伤后再生的轴突如果缺乏髓鞘包绕,其传导信息的功能将受到极大的影响。为了更高效率地修复受损伤脊髓的神经环路,基于促进脊髓白质轴突直行生长及形成髓鞘的需求,他们采取了合成生物学理念和组织工程新技术,设计构建了类脊髓白质组织(类白质)。
2021年10月20日,曾园山教授团队在国际TOP期刊Bioactive Materials(中科院一区,IF=14.593)上在线发表了题为: Construction of a niche-specific spinal white matter-like tissue to promote directional axon regeneration and myelination for rat spinal cord injury repair的研究成果。重点实验室赖碧琴研究员为该论文的第1作者兼共同通讯作者,研究生白瑜蓉为共同第1作者,重点实验室曾园山教授为通讯作者。
类白质的构建遵从了组织器官发育的主要原理,不同于传统意义的类器官,属于工程化的类神经组织。其构建综合了天然生物活性支架、种子细胞、神经营养因子和培养时间,这4个重要因素的相互作用。其中,天然生物活性支架的选择是关键因素。研究表明,相对于胶原、明胶、壳聚糖等单一成分的生物材料,神经组织(如坐骨神经或者脊髓组织)在去细胞后的细胞外基质蛋白能为神经元轴突提供更多促进其生长信号。支架成分越接近脊髓的细胞外基质,越有利于为受损伤脊髓提供促进轴突生长及形成髓鞘的微环境。
在脊髓白质损伤处移植天然生物活性支架引导再生轴突的直行生长显得非常重要。虽然可注射凝胶材料或者纳米微球材料可以达到填补脊髓空洞和促进轴突生长的效果,但对于较大缺损范围的损伤,要引导轴突直行再生则要求支架材料具备直行导向性。本研究结果证实,去细胞视神经可作为类白质构建的优选材料。这种天然生物活性支架的特征在于其微拓扑物理结构,即均匀分布的直行通道和微米级横向小孔,特别适宜再生轴突的直行生长及其侧支出芽,也营造了少突胶质细胞在通道间迁移和信息交流的空间。另一个特征是去细胞视神经独特的细胞外基质能够为少突胶质细胞谱系的定植、分化和功能成熟,提供更适宜的微环境。蛋白质组学检测结果和少突胶质细胞谱系单细胞测序的分析证实了去细胞视神经诱导少突胶质细胞谱系发育和功能成熟的重要机制。
应用去细胞视神经构建的类白质最终实现了与宿主脊髓白质良好整合,使再生轴突得以直行生长和髓鞘化,有效地解决了脊髓白质损伤修复所面临的如何同时促进再生轴突直行生长和髓鞘化的难题,从而促使肢体精细运动和感觉功能得到明显的改善。类白质组织移植修复脊髓白质损伤的主要机制在于其为再生轴突提供了物理引导、细胞外基质、髓鞘形成细胞和神经营养因子。有趣的是,去细胞视神经中富含的层黏连蛋白(laminin, LN)能够与少突胶质细胞所分泌的神经营养素-3(neurotrophin-3, NT-3)亲和结合,营造了局部富集NT-3的微环境,更好地维持促神经再生和髓鞘化的独特生态位[图示]。
组织工程策略的优势在于可针对某种神经组织修复的需求,既可实现工程化神经组织的标准化构建,又可实现个性化的改性,更利于实现临床转化应用。本研究为高效修复脊髓白质损伤提供了组织工程新策略。将来可以在人源化基因编辑猪来源的去细胞视神经支架上种植病人自体iPSC源性神经干细胞,构建用于临床脊髓损伤修复的类脊髓组织。未来的研究中,也可以采取组织工程设计策略将去细胞视神经负载其他类型的功能性种子细胞,或者将去细胞视神经功能改性后用于构建组织工程化的类组织或者类器官,使之满足体外病理和药物研究模型的需求或者满足体内移植修复受损伤组织的需求。
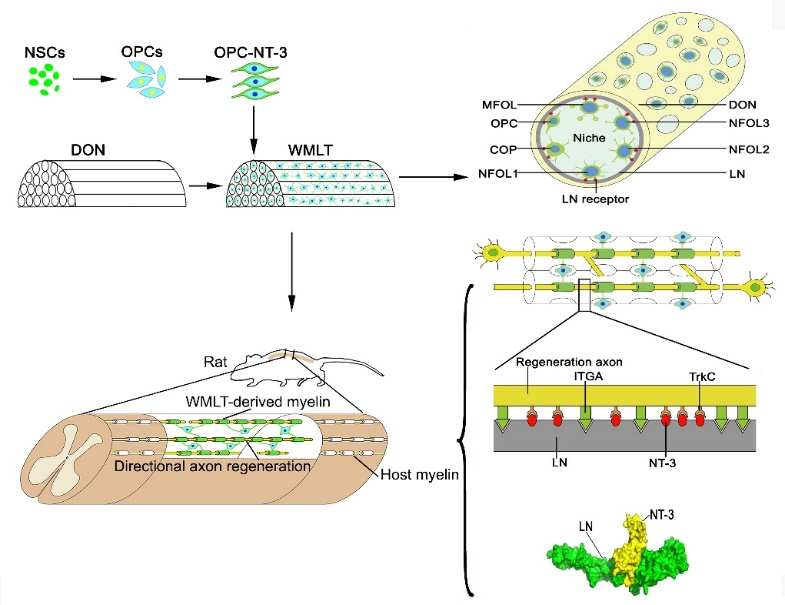
图示: 类白质(WMLT)构建及其移植修复大鼠半横切背侧脊髓损伤的机制。将神经干细胞(NSCs)诱导为少突胶质前体细胞(OPCs),通过基因修饰使之过表达NT-3,再将OPC-NT-3种植于去细胞猪视神经(DON)构建WMLT。WMLT内微环境形成支持少突胶质细胞谱系的定植、分化和功能成熟的独特生态位(ecological niche)。将WMLT移植到半横切背侧脊髓损伤处,DON通道表面的富含的层黏连蛋白(LN)能够和少突胶质细胞所分泌的NT-3亲和结合,营造局部富集NT-3的微环境。LN还能够通过与少突胶质细胞表面和再生轴突表面的整合素(ITGA)通过配体(NT-3)和受体(TrkC)结合的方式引导轴突直行生长和髓鞘化,从而在WMLT移植后与宿主脊髓组织实现更好的结构整合和功能修复。
该课题由国家自然科学基金重大项目(81891003)、国家重点研发计划(2017YFA0104704)和中国科协 “青年人才托举工程”(YESS, 2018QNRC001)资助。
论文链接://authors.elsevier.com/sd/article/S2452-199X(21)00456-4

