Adv Sci|吕志跃团队揭示天然免疫传感器Zbp1通过调控巨噬细胞炎症表型介导广州管圆线虫感染所致的中枢神经系统炎症
中枢神经系统(CNS)炎症是脑胶质瘤、阿尔兹海默病及脑部感染性疾病等多种神经系统疾病的核心病理环节。广州管圆线虫(Angiostrongylus cantonensis,AC)首先由中山大学陈心陶教授于1934年发现并命名,是一种专性入侵宿主中枢神经系统的寄生虫,可引起嗜酸性粒细胞增多性脑膜脑炎或脑膜炎,甚至死亡。当前对于广州管圆线虫病的治疗为常规广谱抗寄生虫药、抗炎、降低颅内压等,治疗效果有限,缺乏特异性靶向治疗,患者常出现不可逆性神经系统损伤。为提升AC所致感染性脑炎治疗效果,亟需进一步阐明其致病分子机制,寻找高效特异的治疗靶点,改善患者预后。
感染性脑炎以复杂的免疫微环境为特征,髓系单核细胞作为最重要的天然免疫细胞之一,介导天然免疫及适应性免疫之间的复杂相互调控。然而,在AC所致感染性脑炎中,髓系单核细胞发挥何种作用及其机制尚不知晓。中山大学吕志跃教授团队于2025年1月24日在中科院一区期刊《Advanced Science》(IF=15.1)上发表了题为 “The Innate Immune Sensor Zbp1 Mediates Central Nervous System Inflammation Induced by Angiostrongylus Cantonensis by Promoting Macrophage Inflammatory Phenotypes” 的最新研究。该研究通过转录组芯片、单细胞测序、基因敲除动物模型等技术,首次揭示了天然免疫传感器——Z-DNA结合蛋白1(Z-DNA-binding protein 1,Zbp1)在AC感染致病的关键作用。
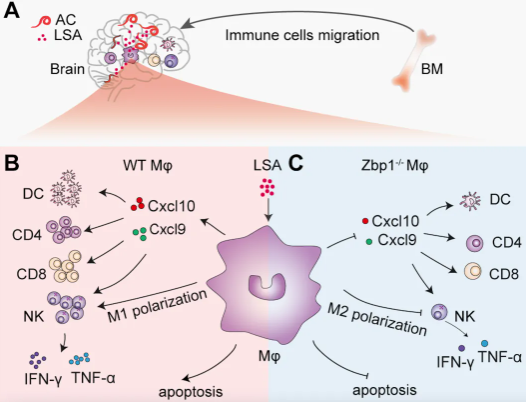
图:Zbp1通过促进巨噬细胞炎症表型介导AC诱导的中枢神经系统炎症
研究团队发现,在AC所致感染性脑炎模型中,骨髓来源的巨噬细胞Zbp1表达上调,并通过与RIPK3直接结合,激活RIP3-MLKL信号轴,促进巨噬细胞的凋亡、M1极化和趋化因子CXCL9与CXCL10的分泌,进而募集免疫细胞并激活CD8+ T细胞及NK细胞分泌TNF-α和IFN-γ,促进AC感染性脑炎的发生发展。而在AC感染的Zbp1敲除小鼠中,巨噬细胞M2型极化增强,凋亡减轻,淋巴细胞(CD4+ T、CD8+ T)浸润及NK细胞毒性显著降低,从而减轻中枢神经炎症反应。
该研究首次证明Zbp1通过诱导凋亡、调控巨噬细胞极化及释放趋化因子,在AC感染引发的中枢神经炎症中发挥重要作用,为寄生虫感染相关的神经免疫互作提供了新的科学依据。不仅进一步阐明了中枢神经系统炎症机制,还为靶向Zbp1-RIP3通路治疗嗜酸性粒细胞增多性神经炎症性疾病提供了新的潜在策略,有望通过抑制Zbp1或其下游信号轴,开发出更加精准有效的广州管圆线虫病治疗手段。
博彩公司排名 吕志跃教授和海南医科大学附属海南省人民医院陈涛教授为共同通讯作者,博彩公司排名 2019级博士生周洪利为该研究论文的第一作者。该研究受国家自然科学基金项目、国家重点研发计划项目和广东省自然科学基金项目等项目资助。吕志跃教授团队长期从事重要病原感染与免疫调控、药物研究等相关方向研究,欢迎对此研究方向感兴趣的博士后和研究生加入。
原文链接:
//advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202413675



